| Ciencias de Joseleg | Química | Química orgánica | Alcoholes
| (Introducción)
(Historia)
(Estructura)
(Nomenclatura)
(Propiedades
físicas) (Propiedades
químicas) (Alcohol
adulterado) (Referencias)
En este capítulo, estudiamos las propiedades físicas y químicas de los alcoholes, una clase de compuestos que contienen el grupo OH- (hidroxilo).
El etanol (CH3CH2OH) es el aditivo en la mezcla de
combustible conocida como E85, el alcohol en las bebidas alcohólicas y un
importante solvente industrial.
Los alcoholes son importantes porque se pueden convertir en muchos otros
tipos de compuestos, incluidos alquenos, haloalcanos, aldehídos, cetonas,
ácidos carboxílicos y ésteres. Los alcoholes no solo se pueden convertir en
estos compuestos, sino que estos compuestos también se pueden convertir en
alcoholes. Así, los alcoholes juegan un papel central en la interconversión de
grupos funcionales orgánicos.
Los grupos hidroxilo se encuentran en carbohidratos y ciertos aminoácidos.
A continuación se presentan dos representaciones de la glucosa, el compuesto
orgánico más abundante en la naturaleza. A la izquierda hay una proyección de
Fischer que muestra la configuración de todos los centros quirales. A la
derecha hay una estructura cíclica, la forma predominante en la que existe esta
molécula tanto en forma sólida como en solución. El aminoácido l-serina es uno
de los 20 bloques de construcción de aminoácidos de las proteínas.
Figura 3‑1. (Izquierda) proyección de fischer de la D-glucosa,
(Centro) fórmula estructural de la β-D-glucosapiranosa, (Derecha) fórmula
estructural de las L-serina.
Los alcoholes se pueden ver estructuralmente de dos maneras:
👉 como derivados hidroxilados de alcanos alquenos o alquinos; y
👉 como derivados de agua alquilada.
El alcohol etílico, por ejemplo, puede ser visto como una molécula de etano en la que un hidrógeno ha sido reemplazado por un grupo hidroxilo o como una molécula de agua en la que un hidrógeno ha sido reemplazado por un grupo etilo.
El grupo hidroxilo
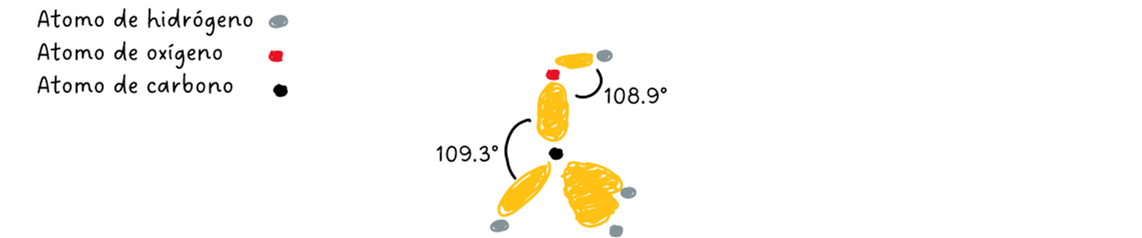
El grupo funcional de un alcohol es un grupo -OH (hidroxilo) unido a un carbono con hibridación sp3. El átomo de oxígeno de un alcohol también tiene hibridación sp3. Dos orbitales híbridos sp3 de oxígeno forman enlaces sigma con átomos de carbono e hidrógeno, y los dos orbitales híbridos sp3 restantes contienen cada uno un par de electrones no compartidos.
Figura 3‑2. Representación en base a la
teoría del enlace de valencia de la molécula de metanol que presenta claramente
la hibridación sp3 del átomo de carbono central y los ángulos de enlace entre
carbono e hidrógenos así como entre oxígeno e hidrógeno.
Alcoholes
primarios
Un alcohol primario es un alcohol en el que el grupo hidroxilo está unido a
un átomo de carbono primario. También se puede definir como una molécula que
contiene un grupo “–CH2OH”, en otras palabras normalmente los
alcoholes primarios son aquellos en los cuales el grupo de hidroxilo se ubica
en una punta terminal de un esqueleto de carbono.
3.1
Observe que la complejidad del grupo alquilo adjunto es irrelevante. En
cada caso, solo hay un enlace a un grupo alquilo del grupo CH2 que
contiene el grupo -OH. Hay una excepción a esto. El metanol, CH3OH, se cuenta
como un alcohol primario aunque no haya grupos alquilo unidos al átomo de
carbono -OH.
Alcoholes
secundarios
Un alcohol secundario es un alcohol en el que el grupo hidroxilo está unido
a un átomo de carbono secundario. También se puede definir como una molécula
que contiene un grupo “–CRHOH”, en otras palabras normalmente los alcoholes secundarios
son aquellos en los cuales el grupo de hidroxilo se ubica al interior de una
cadena pero sin que el carbono en el cual está unido tenga una ramificación extra
con un grupo alquilo.
3.2
Alcohol
terciario
Un alcohol terciario es un alcohol en el que el grupo hidroxilo está unido a un átomo de carbono terciario. También se puede definir como una molécula que contiene un grupo “–CR2OH”, en otras palabras normalmente los alcoholes terciarios son aquellos en los cuales el grupo de hidroxilo se ubica al interior de una cadena y cuyo carbono está unido a una ramificación extra con un grupo alquilo.
3.3
Aunque en términos de nomenclatura el nivel de carbono no es relevante, sí que va a ser muy importante a la hora de estudiar sus propiedades químicas, debido a que existen reacciones que son selectivas con respecto al carbono en el cual se encuentra Unido el grupo hidroxilo. .




No hay comentarios:
Publicar un comentario