| Ciencias de Joseleg | Química | Química orgánica | Ácidos carboxílicos | (Introducción) (Estructura) (Nomenclatura) (Propiedades físicas) (Propiedades químicas) (Importancia) (Mantequilla y margarina) (Referencias)
Acidez
Los ácidos
carboxílicos se disocian en agua para formar iones carboxilato e iones hidronio
(RCOOH → RCOO- + H+). El ion carboxilato (RCOO-)
formado se estabiliza por resonancia mediante una deslocalización efectiva de
la carga negativa, y
además tiende a generar la reacción reversa para regenerar la fórmula molecular
del ácido carboxílico.
Los ácidos
carboxílicos son más débiles que los ácidos minerales pero son los más fuertes
entre los compuestos orgánicos. La acidez de un ácido carboxílico es mayor que
la de los alcoholes e incluso la de los fenoles. Recuerde que el concepto del fortaleza o
debilidad de un ácido se relaciona con la reacción reversa, entre mayor sea la
reacción reversa para regenerar la fórmula molecular del ácido más débil va a
hacer, debido a que va a generar menos iones de hidrógeno para formar
hidrogeniones (H3O+).
Formación de sales con metales
Al igual
que cualquier ácido inorgánico, el anión carboxilato puede reaccionar con
cationes positivos como el sodio, el potasio, o el amonio para formar sales.
Esas sales
orgánicas con metales son muy importantes al nivel industrial pues son
básicamente lo que denominamos vulgarmente como Jabones.
Saponificación
Los jabones
son sales de ácidos grasos de sodio o potasio, producidos a partir de la
hidrólisis de grasas en una reacción química llamada saponificación. Cada
molécula de jabón tiene una larga cadena de hidrocarburo, a veces llamada
"cola", con una "cabeza" de carboxilato. En el agua, los
iones de sodio o potasio flotan libres, dejando una cabeza cargada
negativamente. Marcas Overstolz y Botteram.
Se debe
tener en cuenta que los ácidos orgánicos de cadena larga empleados para la
saponificación normalmente no se encuentran de manera libre en sus materias
primas que normalmente son materias primas de origen biológico. Los seres vivos
tienden a almacenar los ácidos carboxílicos, denominados en ese contexto ácidos
grasos, en paquetes llamados triglicéridos, de allí que la saponificación debe
tener dos pasos, la primera es la liberación del ácido graso del triglicérido, generando
tres ácidos carboxílicos libres y una molécula de glicerol.
De allí que
la saponificación siempre genera 2 productos de importancia industrial, el jabón,
por un lado, y el glicerol por otro.
Carbonatación de un
reactivo de Grignard
Agregar CO2
a un reactivo de Grignard seguido de acidificación proporciona una vía útil
para los ácidos carboxílicos.
Síntesis industrial de
ácido etanoico
El ácido
acético o etanoico es un químico a granel importante que actualmente se produce
a través de la carbonilación de metanol utilizando CO de origen fósil, de allí
que sus precios van a depender de la disponibilidad de petróleo en el mercado.
La síntesis
de ácido acético a partir del CO2 renovable y barato es de gran
importancia industrial y geoestratégica, ya que liberaría a la industria
química, al menos en lo que se refiere al ácido acético, de la disponibilidad
del petróleo en ciertos países, pero las rutas de síntesis química conocidas encuentran
dificultades, especialmente en la selectividad y la actividad de la reacción,
por lo que a 2022 aún no están disponibles industrialmente.
Reducción por hidruro de
litio y aluminio
El hidruro
de litio y aluminio reduce un grupo carboxilo a un alcohol primario.
Esterificación de Fischer
Se puede
preparar un éster tratando un ácido carboxílico con un alcohol en presencia de
un catalizador ácido.
La esterificación de
Fischer es reversible. Para lograr altos rendimientos de éster, es necesario
forzar el equilibrio hacia la derecha. Una forma de lograr esto es usar un
exceso de alcohol; otra es eliminar el agua por destilación azeotrópica
utilizando una trampa Dean-Stark.
Reacción con diazometano
El diazometano se usa
para formar ésteres metílicos a partir de ácidos carboxílicos.
Debido a que el
diazometano es explosivo y venenoso, se usa solo cuando no son adecuados otros
medios para preparar ésteres metílicos.
Conversión a haluros de ácido
Los cloruros de ácido,
los haluros de ácido más comunes y ampliamente utilizados se preparan tratando
un ácido carboxílico con cloruro de tionilo.
Descarboxilación de b-cetoácidos
Los b-cetoácidos se
descarboxilan al calentarse.
Síntesis de triglicéridos
El alcohol glicerol puedes reaccionar
con 3 ácidos carboxílicos para formar triglicéridos. Esa reacción ocurre
principalmente en contextos biológicos y está regulada enzimáticamente.







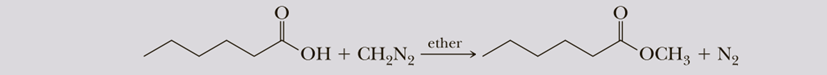



No hay comentarios:
Publicar un comentario