| Ciencias de Joseleg | Química | Química orgánica | Alquinos | (Introducción) (Triple enlace) (Nomenclatura) (Propiedades físicas) (Propiedades químicas) (Importancia biológica) (Referencias)
Con un
grupo funcional reactivo, los alquinos participan en muchas reacciones
orgánicas. Este uso fue iniciado por Ralph Raphael, quien en 1955 escribió el
primer libro describiendo su versatilidad como intermediarios en síntesis
orgánicas artificiales (Raphael, 1955).
Los alquinos experimentan muchas de las mismas adiciones
electrofílicas que los alquenos. Una reacción característica es un enlace pi
que actúa como nucleófilo (atractor
de protones o atractor de cargas positivas) para formar un nuevo enlace
con un electrófilo (atractor
de electrones o atractor de cargas negativas). En esta sección,
estudiamos la adición de bromo y cloro, así como la adición de haluros de
hidrógeno.
Los elementos de H2O también se pueden agregar al
triple enlace carbono-carbono de un alquino mediante las mismas dos reacciones
que se usan para la hidratación de los alquenos, a saber, hidroboración
oxidación e hidratación catalizada por ácido. Aunque los reactivos son
similares, los productos de hidratación de alquenos y alquinos son bastante
diferentes.
Acidez
Una de las
principales diferencias entre la química de los alquinos y la de los alquenos o
alcanos es que un hidrógeno unido a un átomo de carbono con triple enlace de un
alquino terminal es lo suficientemente ácido como para que pueda ser eliminado
por una base fuerte, como la amida de sodio NaNH2, para dar un anión
acetiluro
5.1
Sin embargo las
bases débiles como el agua son incapaces de desproporcionar a los alquinos
terminales, por lo que es muy importante estar pendientes en el enunciado y que
diga la clave base fuerte.
Adición de bromo y cloro
La adición
de un mol de Br2 a un alquino da un dibromoalqueno estereoselectivamente
para formar un alqueno en trans halógenos, sin embargo tenga en cuenta que la
estereoselectividad es proporcional por lo tanto ahora cierto proporción de
producto que se haya formado en su posición cis. Llevar a cabo la bromación en ácido acético con
ion bromuro añadido (por ejemplo, LiBr) aumenta significativamente la
preferencia por la adición en trans.
5.2
Los
alquinos se someten de manera similar a la adición de Cl2, aunque de
manera menos estereoselectiva que con Br2.
Adición de haluros de
hidrógeno
Los
alquinos agregan uno o dos moles de HBr y HCl, dependiendo de las proporciones
en las que se mezclen el alquino y el ácido halógeno.
5.3
Como se
muestra en la Ecuación 5.3, la adición del primer y segundo mol de HBr es
regioselectiva. La adición de haluros de hidrógeno sigue la regla de
Markovnikov; el hidrógeno se suma al carbono que
tiene el mayor número de hidrógenos.
Polimerización de vinilo
La adición
de un mol de HCl al acetileno (etino) da cloroeteno (cloruro de vinilo), un
compuesto de considerable importancia industrial.
5.4
El cloruro
de vinilo es el monómero en la producción del polímero poli(cloruro de vinilo),
comunmente denominado PVC. El PVC domina gran parte del mercado de plomería y
construcción para plásticos. Aproximadamente el 67 % de todas las tuberías,
accesorios y conductos, junto con el 42 % de todos los plásticos utilizados en
la construcción en la actualidad, están fabricados con PVC.
Hidrogenación
Al ser más
insaturados que los alquenos, los alquinos característicamente experimentan
reacciones que muestran que están "doblemente insaturados". Los
alquinos son capaces de agregar dos equivalentes de H2, mientras que
un alqueno agrega solo un equivalente. Dependiendo de los catalizadores y las
condiciones, los alquinos agregan uno o dos equivalentes de hidrógeno. La
hidrogenación parcial, que se detiene después de la adición de un solo
equivalente para dar el alqueno, suele ser más deseable ya que los alcanos son
menos útiles como intermediarios de reacciones orgánicas industriales:
En alquinos la hidrogenación genera un alquenos en cis si se
involucra el reactivo de Lindlar.
5.5
De lo contrario genera el isómero trans, lo cual altera la dirección en la cual se
encuentra el resto de la cadena, generando isómeros.
5.6
La aplicación a mayor escala de esta tecnología es la
conversión de acetileno en etileno en refinerías (el craqueo al vapor de
alcanos produce un pequeño porcentaje de acetileno, que se hidrogena
selectivamente en presencia de un catalizador de paladio/plata). Para alquinos
más complejos, se recomienda ampliamente el catalizador de Lindlar para evitar
la formación del alcano, por ejemplo, en la conversión de fenilacetileno en
estireno.
Hidrogenación por hidroboración
Se trata de
una hidrogenación a 2 pasos cuyo producto final es un alqueno en cis.
5.7
Hidrogenación con metales disueltos
Los alquinos también se pueden reducir a alquenos usando sodio o litio metálico en amoníaco líquido o en aminas primarias o secundarias de bajo peso molecular. El metal alcalino es el agente reductor. La reducción de un alquino a un alqueno mediante litio o sodio en amoníaco líquido, NH3(l), es estereoselectiva; implica principalmente la anti adición de dos átomos de hidrógeno al triple enlace para formar un alqueno trans.
5.8
Hidratación catalizada con ácidos
En presencia de ácido sulfúrico concentrado y sales de
Hg(II) como catalizadores, los alquinos se someten a la adición de agua en una
reacción análoga a la oximercuración de los alquenos. Las sales de Hg(II) más
utilizadas para este propósito son HgO, HgSO4 o Hg(OAc)2.
Para los alquinos terminales, la adición de agua sigue la regla de Markovnikov;
el hidrógeno se suma al átomo de carbono del
triple enlace que lleva el hidrógeno. El enol resultante está en
equilibrio con la forma ceto más estable, por lo que el producto aislado es una
cetona (un aldehído en el caso del propio acetileno).
5.9





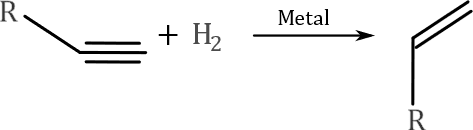



No hay comentarios:
Publicar un comentario